

吉西他滨联合顺铂是晚期转移性或不可手术切除胆道系统肿瘤(BTC)的标准一线治疗,然而该方案的疗效有限。目前PD-1 / PD-L1免疫检查点抑制剂已经在多种肿瘤中取得了显著疗效,但是,在BTC中抗PD-1 / PD-L1抗体的研究还很有限。
为此,中国人民解放军总医院生物治疗科韩为东教授团队开展了纳武利尤单抗(nivolumab)联合吉西他滨和顺铂治疗晚期BTC的临床试验,最新研究成果于2020年6月3日发表于Journal for ImmunoTherapy of Cancer (JITC,IF=8.728) 杂志。裕策生物参与其中的基因检测与数据挖掘工作。
研究设计
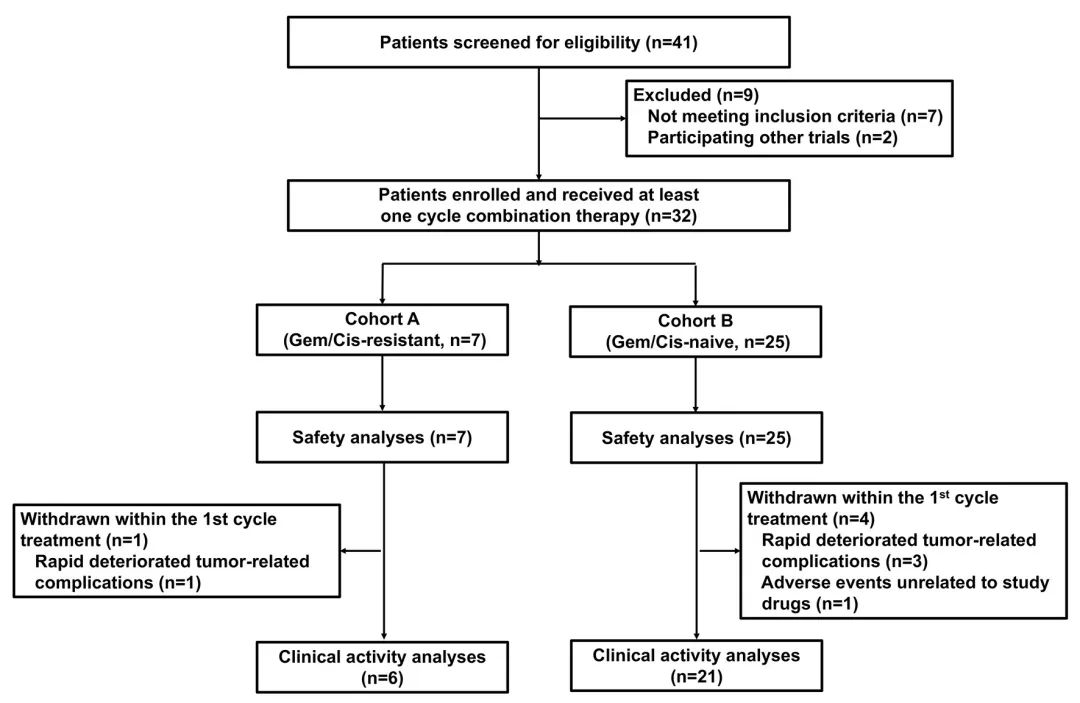
该研究是一项单中心、单臂、开放标签的Ⅱ期临床试验, 旨在明确纳武利尤单抗(nivolumab)联合化疗在晚期BTC中的疗效和安全性。试验共纳入32位(中位年龄为60岁)的不可切除或转移性BTC患者(ECOG评分为0-2)。
队列划分:根据先前的系统疗法划分为两个队列:队列A(既往化疗抵抗)和队列B(未接受过化疗)。
主要研究终点:客观缓解率(ORR)。次要结果包括安全、疾病控制率(DCR)、无进展生存期(PFS)和总体生存期(OS)。
探索性目的:探索生物标志物,以预测临床反应和预后。
治疗方案
所有入组患者均接受联合治疗:吉西他滨1000 mg / m2(第1天和第5天),顺铂75 mg/m2(第1天)和nivolumab 3 mg/kg(第3天),静脉输注,3周一个疗程,最多给予6个疗程治疗。此后,对反应敏感或疾病稳定的患者改用维持治疗,每6-8周给予一次nivolumab和吉西他滨治疗。每次注射药物之前,收集外周血样品,以测试细胞因子的浓度水平。

疗效结果
01 治疗疗效
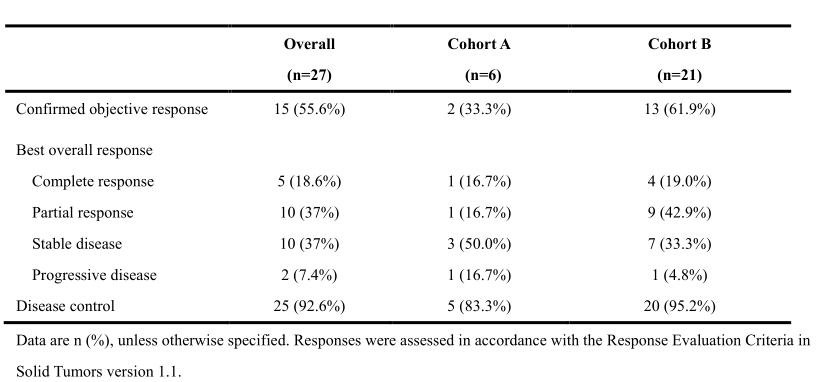
在整个患者群体中,ORR为55.6%,DCR为92.6%。队列A的7例患者中有6例可评估疗效, 其中1例获得CR,1例获得PR ,ORR和DCR分别为33.3%和83.3%。在25例队列B患者中,共21例患者纳入疗效评价,其中13例(61.9%)达到CR或PR,ORR和DCR分别达到61.9%和95.2%。
02 PFS和OS
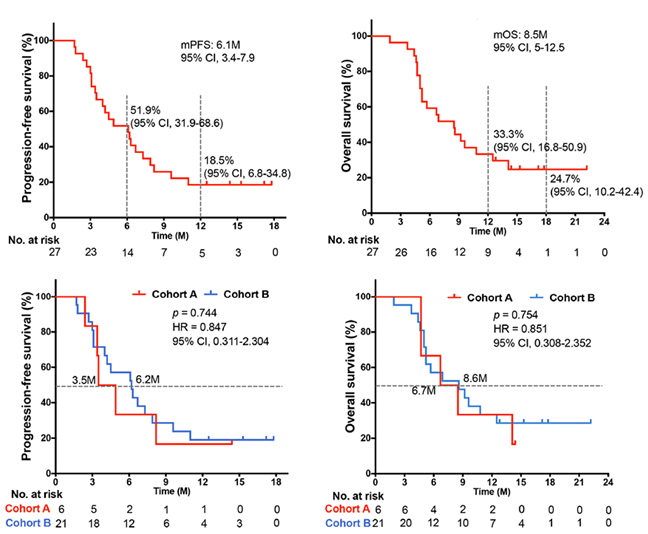
该研究的中位PFS为6.1个月(95%CI,3.4 - 8.2),6个月和12个月无进展的比例分别为51.9%(95%CI,31.9 - 68.6)和18.5%(95%CI,6.8 - 34.8)。中位OS为8.5个月(95%CI,5.0 - 12.5),12个月OS率和18个月OS率为33.3%(95%CI,16.8 - 50.9)和24.7%(95%CI,10.2 - 42.4)。
队列A和队列B的比较显示,相较于化疗进展患者,未接受过化疗的患者可获得更长的中位PFS,但两者之间未显示出显著统计学差异。
03 与治疗有关的毒性
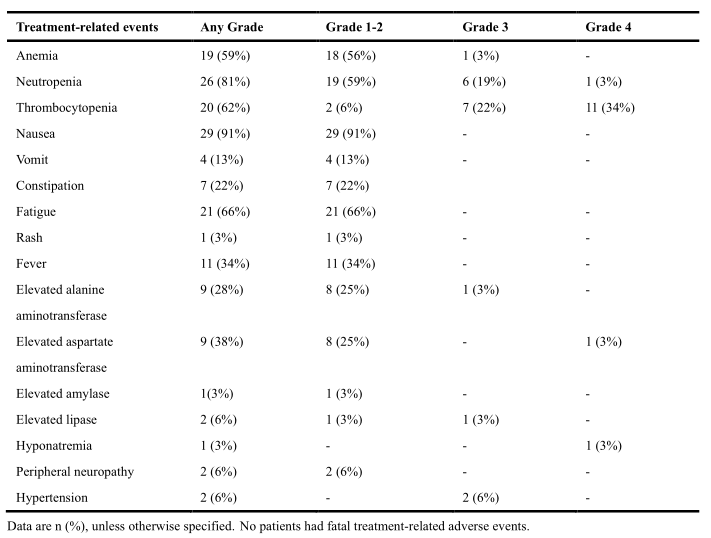
在32名入组患者中,所有患者均经历了至少一项与治疗相关的不良事件。最常见的不良事件为恶心(91%),中性粒细胞减少症(81%),疲劳(66%),血小板减少(62%)和贫血(59%)。最常见的3级以上治疗相关不良反应为血小板减少 (56%),中性粒细胞减少症(22%)。其他严重不良事件还包括3级丙氨酸转氨酶升高(3%),4级天门冬氨酸转氨酶升高(3%),3级脂肪酶升高(3%),3级低钠血症(3%)和3级高血压(6%)。一名患者出现免疫治疗相关不良事件:皮疹(3%)。治疗过程中未出现与治疗相关性死亡。
Biomarker探索
26个(81%)肿瘤样本进行了PD-L1表达评估,其中12个(37%)的PD-L1表达阳性,14个(44%)阴性。PD-L1表达水平与疗效反应、PFS、OS等均未显示出明确的相关性。
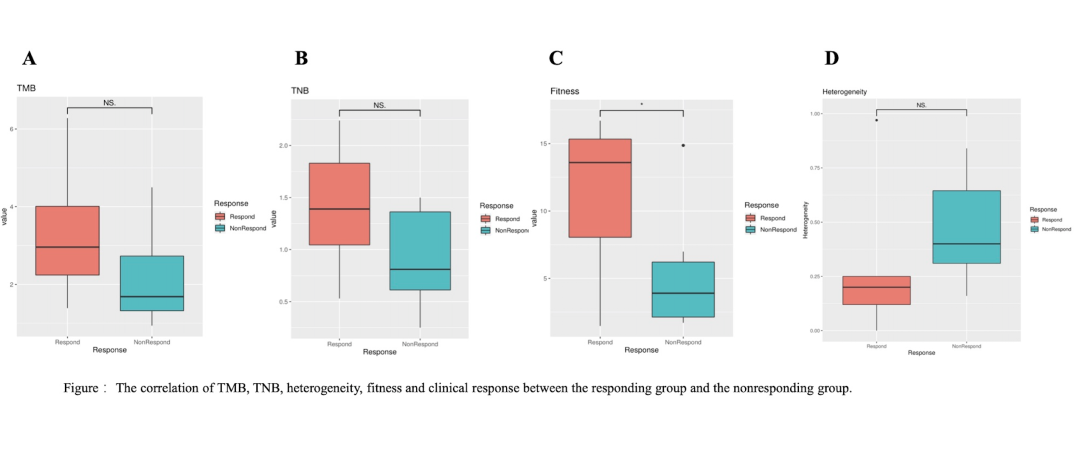
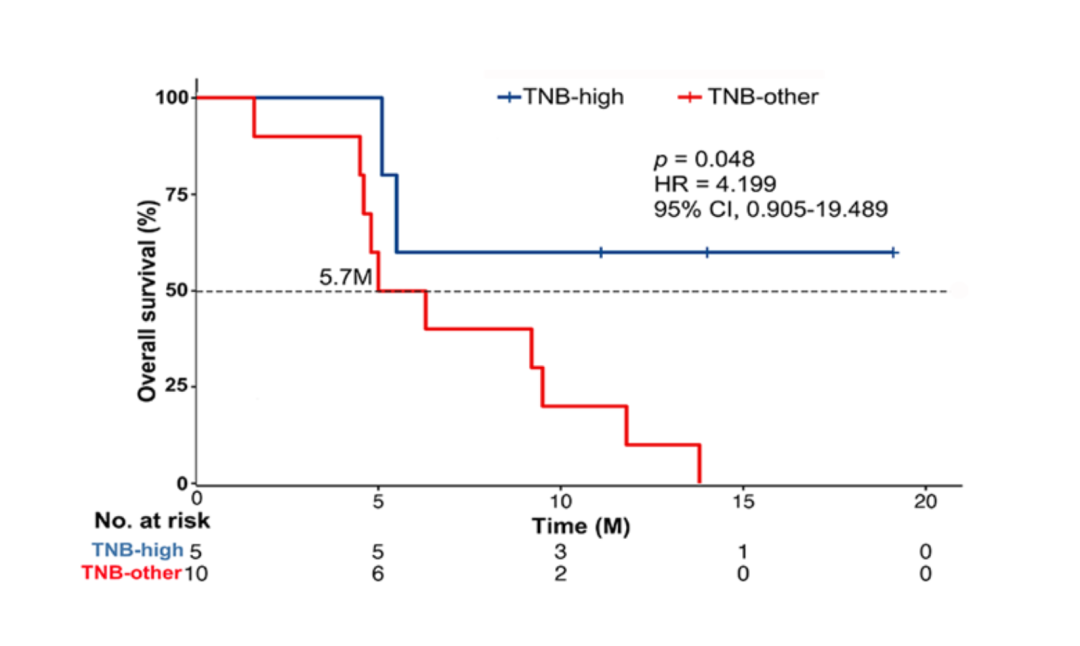
研究表明,应答组(CR+PR)中肿瘤突变负荷(TMB),新生抗原负荷(TNB)和肿瘤适合性模型评分(fitness score)均高于非应答组(SD+PD),而肿瘤异质性(intra-tumor heterogeneity)在应答组中较低,在这些指标中fitness score具有统计差异(p = 0.041)。另外TNB (cutoff = 1.37 neo/ Mb)具有预后价值,TNB > 1.37的患者的OS明显长于TNB<1.37的患者(p = 0.048)。
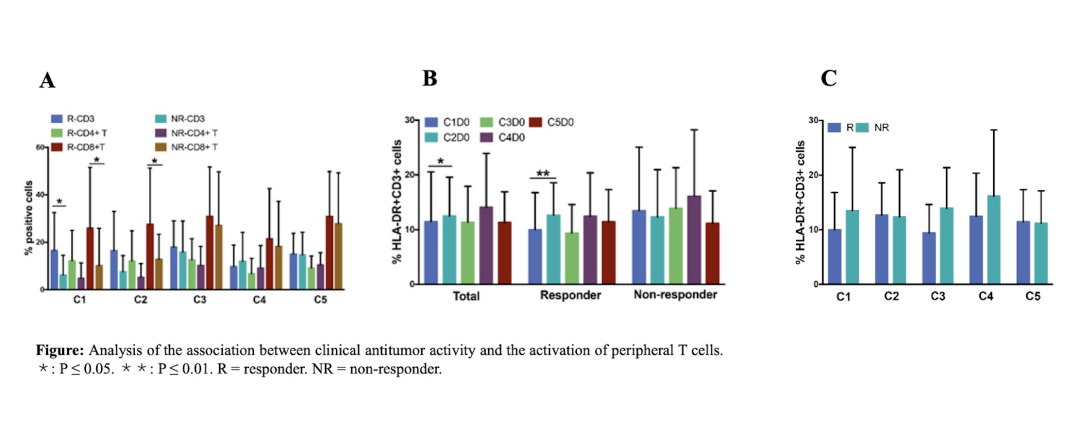
对治疗过程中外周血T细胞变化的分析表明,应答组中基线血液的CD3 +T细胞的基线比例高于非应答组中的比例(p = 0.046)。联合治疗开始后,患者外周血中HLA-DR+CD3+T细胞的比例增加,特别是在客观反应患者中(p = 0.009),但在应答者和非应答者之间未观察到统计学差异。
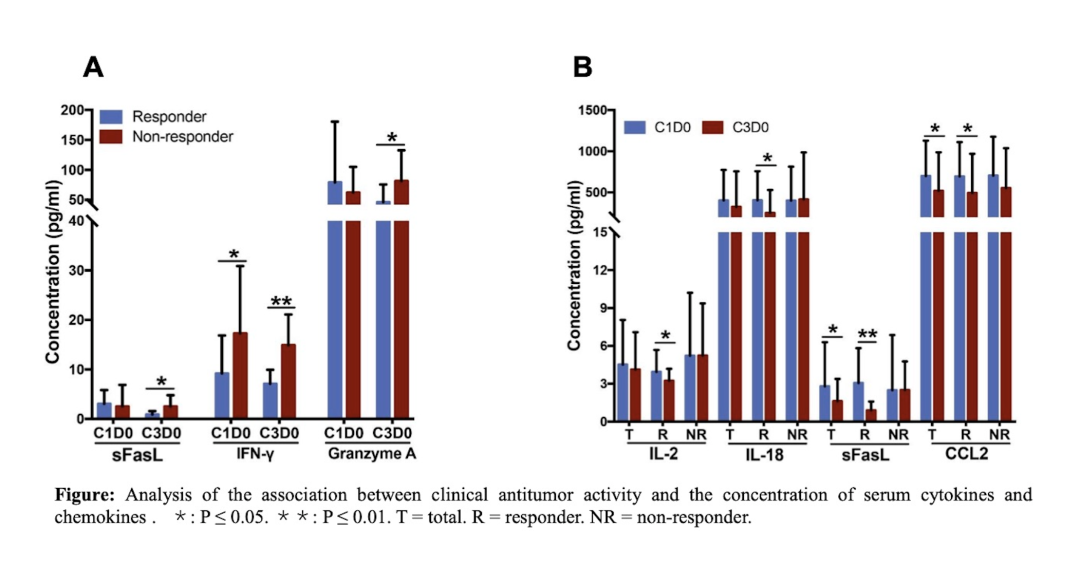
此外研究者还进行了基线(C1D0)和两疗程后(C3D0)外周血清细胞因子和趋化因子的变化与临床响应之间的关联性分析。联合治疗2个周期后,非应答组血清sFasL和颗粒酶A的浓度均高于应答组(p = 0.042和0.048),而应答组中的IL-2、IL-18、sFasL和CCL2的浓度与非应答组相比显着下降(P = 0.036、0.047、0.012和0.042)。
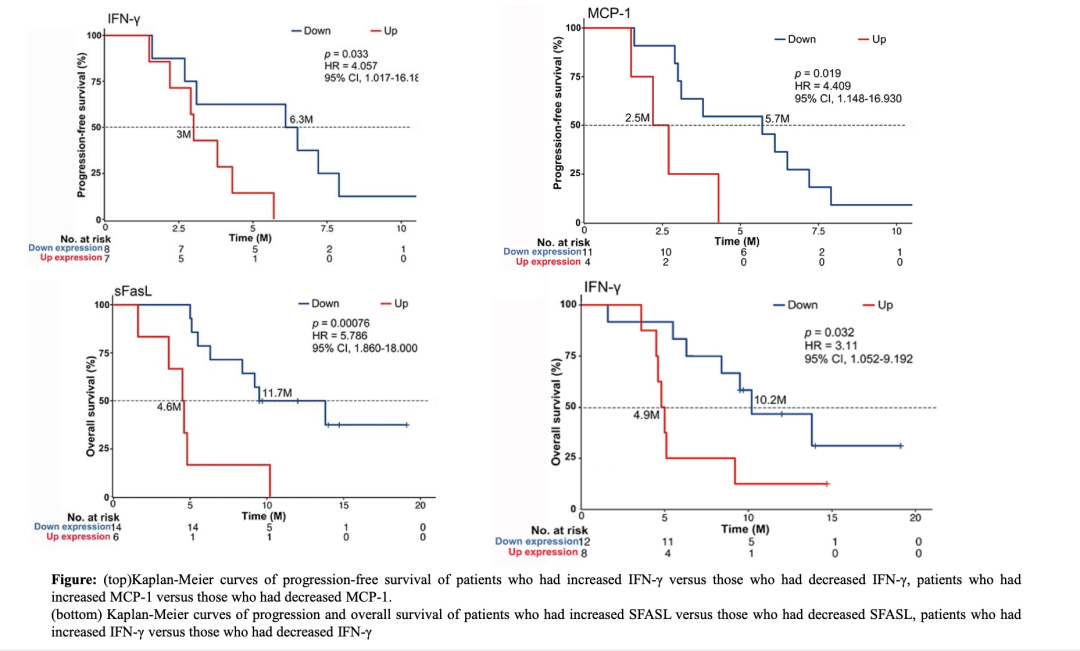
进一步分析发现,联合治疗后IFN-γ和MCP-1浓度降低的患者比治疗后浓度升高或保持相同水平的患者可获得更长的PFS(p = 0.033和p = 0.019);治疗后血清sFASL和IFN-γ水平下降患者中可获得更长的OS(分别为p = 0.00076和 0.032)。
总结
本研究表明nivolumab联合吉西他滨和顺铂在晚期不可切除或转移性BTC中具有良好的抗肿瘤疗效和可控的安全性,但相较于化疗,临床预后数据未显示出显著提高。而biomarker的探索研究发现:
1.较高的TMB和TNB和较低的肿瘤异质性可能会有更好的临床反应;
2.发现基线血液中较高的基线CD3+T细胞比例和治疗过程中外周血IL-2、IL-18、sFasL和CCL2水平的降低可能预示基于ICI的联合治疗的更好结果;
3.治疗前TNB较高的患者可获得更长的OS。受样本量与非随机设计的限制,这项初步研究的结果尚需后续更大样本量的随机对照临床试验确认。
专家点评
01韩为东主任
胆管癌是目前肿瘤治疗领域的临床难题之一,尤其是对于不可手术切除或复发转移患者,长期以来没有很突出的治疗方案。本团队近年来针对这类患者进行了一些前瞻性探索性临床研究。
我们之前的结果显示,相较于传统治疗手段,CAR T细胞治疗的临床疗效方面有所提高,主要结果发表于Clinical Cancer Research与Protein & Cell杂志。本次发表的是关于化疗联合免疫疗法治疗胆管癌的II期临床试验结果,尽管是单臂研究,但获得了比较乐观的结果,初步证实了联合PD1抗体对于客观缓解率与生存率的提升。
综合看,本团队的几项研究基本上可以说明免疫治疗在胆管癌的治疗中具有进一步发展的空间。回到本研究,由于患者对免疫治疗响应的差异性,我们也试图寻找可以有效预测疗效的分子特征与标记,文中可以看到除了血清学分子与疗效关联外,肿瘤本身的生物学分子特征与免疫治疗之间的关联性值得进一步完善数据挖掘。
02赵海涛主任
近期中国人民解放军总医院第一医疗中心韩为东教授团队在J Immunother Cancer上发表的使用免疫检查点抑制剂纳武利尤单抗(Nivolumab)联合吉西他滨和顺铂化疗在不能切除或转移性胆管癌(BTC)的有效性和生物标志物的2期临床研究。本研究共入组32名患者,多数病人存在肝转移,分为化疗进展组(cohort A)及化疗初治组(cohort B)。
本研究的主要终点是客观应答率(ORR),总的而言,ORR能达到55.6%,且在化疗初治组疗效更好,疾病控制率为92.6%,这在晚期胆管癌中是难能可贵的。其他指标结果:中位无疾病进展生存(PFS)和总生存(OS)为6.1个月和8.5个月。最常见的3级或以上不良事件还是和化疗相关,如血小板减少(56%)和中性粒细胞减少(22%)等。
本研究和日本学者在Lancet Gastroenterol Hepatol[1]报道结果类似。更重要的是,该研究探索了疗效的生物标志物,通过对肿瘤样本进行了全外显子测序(WES),PD-L1表达的检测及外周血的细胞因子的检测。发现新抗原适应度(Fitness)可能是预测临床应答的生物标志物。治疗前新生抗原负荷(TNB)高和治疗前后血清可溶性FasL、MCP-1、IFN-γ的变化与预后相关。为患者人群分层管理及后期的更大规模的临床试验提供了依据,期待基于此研究的更大规模的临床研究进行造福晚期胆管癌患者。
点评专家介绍

韩为东
解放军总医院生物治疗科主任、教授
临床肿瘤学博士研究生导师
国家百千万人才
首都科技创新领军人才
原总后勤部科技新星
重点研究方向
主要从事肿瘤治疗抵抗机制与肿瘤免疫治疗的临床研究。先后承担科技部重大专项1项,973课题2项、863项目3项、国家自然基金重大项目1项,重点项目2项,面上项目7项,北京市生物技术前沿项目1项,获得企业投资3项,4项临床治疗技术企业转让。国家发明专利20余项。主编专著3部。
论文研究方向
以第一作者或通讯作者发表SCI论文160余篇,累计影响因子740余分。参与获得省部级二等奖以上4项。2015年,成立了中国研究型医院生物治疗学专业委员会(二级学会),并担任首届主任委员。

赵海涛
北京协和医院肝脏外科主任医师
教授、博士生导师
兼任
2017年国家万人计划专家(领军人才)
2016年国家青年科技创新领军人才
2011年教育部新世纪优秀人才
919肿瘤精准免疫治疗公益基金创始人
北京大学校友会理事
欧美同学会医师协会副秘书长
欧美同学会医师协会青委会主委
欧美同学会医师协会肝胆分会秘书长、副主委
科技部重大项目评审专家
HBSN(SCI收录3.45)杂志副主编
WJG(IF:3.3)杂志编委
以通讯作者发表SCI论文超过70篇
总影响因子超过400分
作者介绍

丰恺超
中国人民解放军总医院生物治疗科
主治医师
北京医学奖励基金会肺癌医学青年专家委员会委员
擅长常见肿瘤的免疫治疗、靶向治疗、I/II期临床试验
重点研究方向
1.免疫检查点抑制剂治疗晚期恶性肿瘤;
2.嵌合抗原受体(CAR)T细胞治疗晚期实体肿瘤及恶性血液肿瘤;
3.表观遗传学药物逆转免疫检查点抑制剂耐药及增敏增效的研究。
论文发表情况
已发表SCI论文10余篇,其中以第一作者发表6篇,发表于Clin Cancer Res、J Hematol Oncol、Protein& Cell、Cellular & Molecular Immunology等期刊,影响因子>30

刘洋
解放军总医院生物治疗科副主任医师
血液肿瘤学硕士,肿瘤学博士
兼任
中国研究型医院学会生物治疗专业委员会委员
中国医药生物技术协会医药生物技术
临床应用专委会委员
青年学组副组长
重点研究方向
专注于淋巴瘤、肝胆胰恶性肿瘤的表观遗传学药物、免疫联合方案和CAR-T细胞的临床研究。
论文发表情况
以第一负责人承担和参与院、国家级课题多项;专利2项;第一作者发表论文21篇,SCI论文11篇,单篇最高影响因子26.3分。参与编撰专著3部。获解放军总医院科技进步二等奖1项。

梅 倩
医学遗传学博士
北京市科技新星
解放军总医院生物治疗团队副研究员
兼任
中国研究型医院学会生物治疗专业委员会青年委员
享受军队优秀专业技术人才三类岗位津贴
入选解放军总医院首批新秀人才
院首批优青培育对象
第六届“总医院十杰青年”
重点研究方向
主要从事肿瘤免疫治疗相关调控机制与临床转化研究,作为主要负责人开展了低剂量去甲基化药物为基础综合方案治疗复发、难治实体瘤国际临床试验,目前已启动10家三甲医院参与的多中心临床研究。
论文发表情况
以第一作者或通讯作者发表SCI论文14篇,总影响因子超80分,单篇最高10.199。主持国家及省部级课题5项及医院人才类基金2项,资助金额300万元;骨干承担十三五国家重点研发计划1项。
参考文献:
[1] Ueno M, Ikeda M, Morizane C, Kobayashi S, Ohno I, Kondo S, et al. Nivolumab alone or in combination with cisplatin plus gemcitabine in Japanese patients with unresectable or recurrent biliary tract cancer: a non-randomised, multicentre, open-label, phase 1 study. Lancet Gastroenterol Hepatol.
Copyright©2021
Shenzhen yucebio Technology Co., Ltd. all rights reserved
Yueicp no.16128839

